Resolución (INV) 34/14.
Del 24/10/2014. 30/10/2014. Oficialízase el Método de “DETERMINACION DE
ACIDO SHIKÍMICO EN VINOS POR CROMATOGRAFIA LIQUIDA DE ALTO RENDIMIENTO Y
DETECCION UV” que, junto a su VALIDACION, obran como Anexo de la
presente resolución.
Mendoza, 24/10/2014
VISTO el Expediente Nº S93:0001809/2014 del Registro del INSTITUTO
NACIONAL DE VITIVINICULTURA y la Resolución OENO Nº 33 de fecha 30 de
julio de 2004, y
CONSIDERANDO:
Que por el expediente citado en el Visto, Departamento Normas Analíticas
Especiales dependiente de Subgerencia de Investigación para la
Fiscalización de Gerencia de Fiscalización del INSTITUTO NACIONAL DE
VITIVINICULTURA (INV) tramita la oficialización del Método de
Determinación de Acido Shikímico en Vinos por Cromatografía Líquida de
Alto Rendimiento y Detección UV.
Que dicha determinación individual o como complemento a otros sistemas
analíticos, posibilita el control de la autenticidad de vinos en
relación a la variedad que le dio origen a través de la determinación
del contenido de ácido shikímico por Cromatografía Líquida de Alto
Rendimiento (CLAR/HPLC).
Que desde 2004 esta determinación es método oficial de la ORGANIZACION
INTERNACIONAL DE LA VIÑA Y EL VINO (OIV).
Que la REPUBLICA ARGENTINA es país miembro de la OIV, representación
ejercida por el INV, y ha participado en la aprobación de este método.
Que el mencionado método ha sido validado con la participación de
Laboratorios de reconocido prestigio internacional y dicha validación ha
sido publicada conjuntamente con el método en la Resolución OENO Nº 33
de fecha 30 de julio de 2004.
Que el referido procedimiento, al utilizar el banco de datos de origen
indudable de contenido de ácido shikímico, permite evaluar la
autenticidad varietal por análisis comparativo o discriminante.
Que esta determinación tiene el respaldo científico suficiente como para
adoptarse como norma de control oficial por este Organismo.
Que Subgerencia de Asuntos Jurídicos del INV ha tomado la intervención
de su competencia.
Por ello, y en uso de las facultades conferidas por las Leyes Nros.
14.878 y 24.566 y el Decreto Nº 1.306/08,
EL PRESIDENTE DEL INSTITUTO NACIONAL DE VITIVINICULTURA
RESUELVE:
1° — Oficialízase el Método de “DETERMINACION DE ACIDO SHIKÍMICO EN
VINOS POR CROMATOGRAFIA LIQUIDA DE ALTO RENDIMIENTO Y DETECCION UV” que,
junto a su VALIDACION, obran como Anexo de la presente resolución.
2° — La adopción del presente método, entrará en vigencia a partir del
día siguiente al de publicación del presente acto administrativo en el
Boletín Oficial de la REPUBLICA ARGENTINA.
3° — Regístrese, comuníquese, publíquese, dése a la Dirección Nacional
del Registro Oficial para su publicación y cumplido, archívese. — C.P.N.
GUILLERMO DANIEL GARCIA, Presidente, Instituto Nacional de
Vitivinicultura.
ANEXO A LA RESOLUCION Nº C.34/14
DETERMINACION DE ACIDO SHIKÍMICO EN VINOS POR CROMATOGRAFIA LIQUIDA
DE ALTO RENDIMIENTO (CLAR/HPLC) Y DETECCION UV
1. DESCRIPCION
El contenido de ácido shikímico en vinos se expresa en unidades de
concentración: MILIGRAMO POR LITRO ELEVADO A LA MENOS UNO (mg.L-1). El
método se aplica para la determinación cuantitativa en un rango de
concentraciones de 5 mg.L-1 a 100 mg.L-1.
2. PRINCIPIO DEL METODO
El ácido shikímico se determina directamente, sin preparación de
muestra, por cromatografía líquida de alta resolución, mediante un
sistema de columnas.
En un primer paso, se realiza una separación preliminar de los ácidos
orgánicos contenidos en el vino sobre una columna de fase inversa de
tipo Octa Decil Silano (ODS), la segunda columna es de tipo
intercambiadora de cationes. Esta última se calienta a 65 °C.
Se utiliza como solvente de elución ácido Sulfúrico 0,02 N (fase móvil),
se obtiene una buena resolución del ácido shikímico, no observándose
interferencia de la matriz del vino. Debido a la doble ligadura del
ciclohexeno, el ácido shikímico presenta un máximo de absorción a los
210 nm lo cual permite ser detectado por un detector UV.
3. REACTIVOS - PATRONES
a) Acido shikímico (CAS 138-59-0), de una pureza mayor o igual al 99%
como mínimo.
b) Acido sulfúrico (H2SO4) P.A., pureza 98 g % g.
c) Agua grado HPLC o tri-destilada: conductividad eléctrica 0,4 a 0,9 µS
a 25 °C; pH 5,1 a 5,5.
d) Etanol absoluto o de pureza = 95% vol.
4. MATERIALES Y EQUIPOS
a) MATERIALES:
I. Matraz aforado de 2.000 ml.
II. Matraz aforado de 1.000 ml.
III. Matraz aforado de 100 ml.
IV. Matraz aforado de 50 ml.
V. Pipeta de doble aforo de 20 ml.
VI. Pipeta de doble aforo de 10 ml.
VII. Pipeta de doble aforo de 25 ml.
VIII. Pipeta automática 1:5.
IX. Propipeta.
X. Filtro de Nylon de poro de 0,22 µm por 47 mm de diámetro.
Xl. Jeringas descartables de volumen variable.
XII. Filtros de jeringa de 0,45 µm de nylon o Fluoruro de Polivinilideno
(PVDF).
XIII. Frasco de cierre hermético tipo Genna o equivalente.
XIV. Viales de vidrio de 1,5 ml con septa pre-ranurada o equivalente.
XV. Papel de filtro técnico: Velocidad de filtración media-rápida -
Densidad 60 a 65 g/m2.
b) EQUIPOS:
I. Sistema de filtración al vacío Millipore o equivalente.
II. Balanza analítica.
III. Heladera (temperatura 1 °C a 10 °C).
IV. Cromatógrafo Líquido de Alto Rendimiento (CLAR/HPLC) compuesto por
los siguientes módulos:
i. Detector UV-VIS.
ii. Rulo (loop) de inyección automática de 100 µl.
iii. Sistema de bombas que permita flujo programable y constante con una
precisión máxima.
iv. Calefactor u horno que permita calentar una columna de intercambio
de 300 mm a 65 °C.
v. Sistema de integración de datos.
vi. Sistema de columnas analíticas:
• Columna de acero inoxidable de fase reversa:
- Marca: Phenomenex.
- Modelo: Luna 5 µ.
- Material de la fase estacionaria: esférico ODS.
- Tamaño de poro: 100 Å
- Largo: 250 mm.
- Diámetro: 4,60 mm.
- Diámetro de partículas: 5 µm.
• Pre-columna para columna de fase reversa compuesta por:
-- Carcasa (holder):
- Marca: Phenomenex.
- Descripción: SecurityGuard / Guard Cartridge Kit.
-- Cartucho o precolumna:
- Marca Phenomenex.
- Largo: 4 mm.
- Diámetro interno: 3 mm.
- Material: ODS.
• Columna intercambiadora de cationes de acero inoxidable:
- Marca: Phenomenex.
- Modelo: Rezex Organic Acid H+.
- Largo: 300 mm.
- Diámetro: 7,80 mm.
• Pre-columna para columna intercambiadora de cationes.
- Marca: Phenomenex.
- Modelo: Rezex Organic Acid H+.
- Largo: 50 mm.
- Diámetro: 7,80 mm.
NOTA: Las marcas y modelos de las columnas pueden reemplazarse siempre y
cuando cumplan con las características de relleno y dimensionales
indicadas.
Las condiciones analíticas pueden variar de acuerdo al equipamiento
utilizado siempre que se compruebe una adecuada performance del sistema.
5. CONDICIONES AMBIENTALES
El equipo HPLC requiere de una instalación que contemple las siguientes
condiciones ambientales para mantener su rendimiento:
a) El laboratorio donde el instrumento se encuentre instalado debe estar
ventilado.
b) Evitar la presencia de polvos o gases corrosivos.
c) Mantener alejado de equipamiento que genere campos magnéticos
fuertes.
d) La temperatura de la habitación debe encontrarse entre 4 °C y 35 °C
con variaciones mínimas durante el día.
e) Las corrientes de aire acondicionado frío-calor no deben dar
directamente sobre el equipo.
f) No exponer a la luz solar directa.
g) Evitar vibraciones.
h) Humedad entre el 20% y el 85%.
i) Evitar condensaciones sobre el equipo.
6. TECNICA
a) Preparación de soluciones:
I. Solución H2SO4 1 N
Colocar en un matraz aforado de 1.000 ml un volumen aproximado de 250 ml
de agua tridestilada, luego agregar 27,2 ml de Acido sulfúrico 98 g % g,
y llevar a volumen con el mismo agua. Conservar la solución con rótulo
indicando contenido, concentración, fecha de preparación y nombre de los
analistas responsables.
II. Solución de elución H2SO4 0,02 N
Colocar en un matraz aforado de 1.000 ml un volumen aproximado de 250 ml
de agua tridestilada, luego tomar 20 ml de la solución de Acido
sulfúrico 1 N y llevar a volumen con el mismo agua. Filtrar la solución
de elución por sistema de filtración con filtro de nylon de poro de 0,22
µm. Conservar la solución en heladera con rótulo indicando contenido,
concentración, fecha de preparación y nombre de los analistas
responsables. En caso que se utilice luego de DOS (2) o más días
posteriores a su preparación, previamente se debe re-filtrar.
b) Preparación de la solución madre patrón de 100 mg. L-1 de ácido
shikímico:
I. Solución hidroalcohólica al 12% vol.
Tomar una probeta de 250 mI, medir 31,25 ml de Etanol (para 96% vol.), y
enrasar con agua tridestilada. En el caso de utilizar etanol de una
pureza distinta a 96% vol., se recalcula el volumen 1 según el siguiente
cálculo: C1.V1=C2.V2.
II. Solución primaria estándar 100 mg. L-1 de ácido shikímico
Pesar 10 mg de ácido shikímico pureza = 99%, transferir
cuantitativamente a un matraz aforado de 100 ml, llevar a volumen con
solución hidroalcohólica al 12% vol. y agitar. Conservar la solución
primaria en heladera con rótulo indicando contenido, concentración,
fecha de preparación y nombre de los analistas responsables.
Conservar el patrón de ácido shikímico en un espacio fresco, con el
envase herméticamente cerrado en un lugar seco y ventilado.
c) Preparación de los estándares (5, 25 y 50 mg. L-1 de ácido shikímico):
I. Estándar de 5 mg.L-1 de ácido shikímico
Tomar un volumen de 2,5 ml de la solución primaria, transferir
cuantitativamente a un matraz aforado de 50 ml, llevar a volumen con
solución hidroalcohólica al 12% vol. y agitar. Conservar el estándar en
heladera con rótulo indicando contenido, concentración, fecha de
preparación y nombre de los analistas responsables.
II. Estándar de 25 mg.L-1 de ácido shikímico
Tomar un volumen de 12,5 ml de la solución primaria, transferir
cuantitativamente a un matraz aforado de 50 ml, llevar a volumen con
solución hidroalcohólica al 12% vol. y agitar. Conservar el estándar en
heladera con rótulo indicando contenido, concentración, fecha de
preparación y nombre de los analistas responsables.
III. Estándar de 50 mg.L-1 de ácido shikímico
Tomar un volumen de 25 ml de la solución primaria, transferir
cuantitativamente a un matraz aforado de 50 ml, llevar a volumen con
solución hidroalcohólica al 12% vol. y agitar. Conservar el estándar en
heladera con rótulo indicando contenido, concentración, fecha de
preparación y nombre de los analistas responsables.
d) Preparación de la muestra:
La muestra de vino tranquilo se toma con jeringas descartables, luego se
le anexa el filtro de membrana de 0,45 µm y con las DOS (2) primeras
porciones de filtrado se enjuaga el vial, descartándose dicho contenido,
la tercer porción es la que se utiliza para la determinación. Previo al
llenado del vial se lo identifica con el número de ingreso de muestra
asignado.
En el caso de vinos con presencia de anhídrido carbónico en solución,
tales como espumantes, gasificados o frizantes, es necesario un
tratamiento previo de desgasificación, mediante filtración con el uso de
papel de filtro, como se indica a continuación:
Se coloca una porción de papel de filtro en un embudo sobre un
Erlenmeyer para recibir el líquido filtrado. A posteriori se somete a
una filtración de membrana al igual que un vino tranquilo.
e) Procedimiento analítico:
I. Inyección de la muestra
Se procede a la colocación de la/s muestra/s en el autoinyector del
cromatógrafo HPLC con los siguientes parámetros de operación:
i. Volumen de inyección: 5 µL.
ii. Flujo: 0,6 ml/min.
iii. Calentamiento de la columna intercambiadora de cationes a 65 °C.
iv. Tiempo mínimo necesario para la estabilización inicial del sistema:
30 minutos.
v. Longitud de onda de detección: 210 nm.
II. Funcionamiento de los sistemas cromatográficos
La respuesta del sistema cromatográfico se evalúa diariamente, a través
de la respuesta del detector y la columna según se describe a
continuación, y periódicamente en función de lo descripto en el
procedimiento de Aseguramiento de la Calidad.
i. Verificación diaria:
• Detector
- Linealidad: se verifica a través de la observación del trazado de la
línea base, la cual debe ser siempre lineal.
- Respuesta: el estudio se realiza a través del análisis de un estándar
de ácido shikímico, de concentración conocida, previo a la inyección de
muestra, verificando la relación de área y concentración obtenida.
• Columna
- Simetría: el estudio se realiza a través del análisis de un estándar
de ácido shikímico, de concentración conocida, previo a la inyección de
muestra, verificando que el pico posea forma de campana de Gauss.
ii. Análisis:
Las inyecciones para la determinación de ácido shikímico se realizan en
el orden de Patrones, Muestras a analizar y Fase Móvil.
• Secuencia de inyección
- Patrones.
Se inyectan los estándares de ácido shikímico de concentración 5, 25, 50
y 100 mg.L-1, con los cuales se realiza la curva de calibración.
-- Muestras a analizar - Fase Móvil
Luego de cada inyección de muestra de vino es necesario un tiempo de
equilibración con el fin de que todas las sustancias del vino hayan sido
bien eluídas. Este tiempo es de TREINTA (30) minutos y se realiza en las
mismas condiciones de análisis haciendo circular fase móvil por el
sistema.
f) Procesamiento de datos:
I. Preparación de la curva de calibración
La determinación cuantitativa de ácido shikímico en las muestras es
efectuada siguiendo el método de calibración externa.
La etapa de calibración y la obtención de la concentración de analito en
una muestra constan de los siguientes pasos:
i. Paso 1: Preparación de los patrones [según punto 6. b) y c)].
ii. Paso 2: Obtención de la relación señal-concentración.
Se traza un gráfico con las señales (área del pico) frente a la
concentración de analito y se calcula la recta que se ajusta a los datos
mediante cálculo por mínimos cuadrados. De esta forma se obtiene la
pendiente (a) y la ordenada al origen (b) que definen la recta. El
cálculo de ajuste por mínimos cuadrados se realiza automático con el
software que acompaña al equipo HPLC o manualmente mediante el uso de
hoja de cálculo Excel.
iii. Paso 3: Uso de la recta de calibrado (cálculos).
Mediante la señal analítica obtenida para las muestras desconocidas, se
interpola en la recta de calibrado para obtener el valor de
concentración de ácido shikímico.
Esta interpolación la realiza automáticamente el software que acompaña
el equipo HPLC. Manualmente, en función de los datos obtenidos (“a” y
“b”) de la curva de calibración, el valor de la concentración se calcula
de la siguiente manera:
Donde:
x= concentración de ácido shikímico en mg.L-1 de la muestra.
y= área correspondiente al pico de ácido shikímico de la muestra.
a= pendiente de la curva de calibración.
b= ordenada al origen de la curva de calibración.
Los resultados, en concentración de ácido shikímico, se expresan en mg.L-1
con DOS (2) cifras significativas.
7. VALIDACION
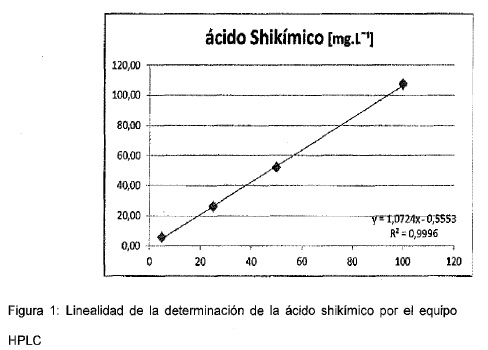
a) Linealidad de la respuesta
Se ha preparado una serie de patrones en un intervalo de 5 a 100 mg.L-1
de ácido shikímico en solución hidroalcohólica al 12%. Cada solución fue
analizada CINCO (5) veces.
El intervalo de linealidad del método está comprendido entre 5 y 100
mg.L-1 como muestra la recta de calibrado de la Figura 1.
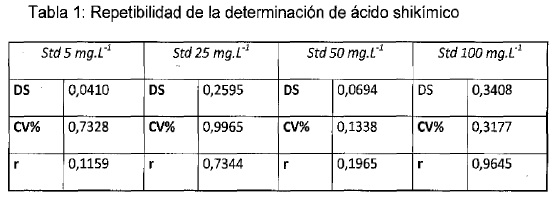
b) Repetibilidad
La repetibilidad (r) de la determinación de ácido shikímico en los
vinos, se ha determinado a partir de los resultados obtenidos en VEINTE
(20) muestras de estándares de ácido shikímico y analizadas CINCO (5)
veces seguidas de manera que estuvieran en condiciones idénticas. Los
resultados se muestran en la Tabla 1:
c) Reproducibilidad
La reproducibilidad (R) de la determinación del ácido shikímico en
estándares en solución hidroalcohólica CINCO (5) veces en diferentes
fechas. Los resultados se dan en la Tabla 2.
REFERENCIAS
[1] Römpp Lexikon Chemie-Versión 2.0, Stuttgart/New York, Georg Thieme
Verlag 1999.
[2] Wallrauch S., Flüssiges Obst 3, 107 - 113 (1999).
[3] 44th session SCMA, 23-26 march 2004, comparison of HPLC, GC, and GC-MS
determination of Shikimic acid in wine, FV 1193.
[4] Resolución Nº OENO 33 de fecha 30 de julio de 2004 de la
ORGANIZACION INTERNACIONAL DE LA VIÑA Y EL VINO (OIV). Dosificación del
ácido shikímico en el vino por Cromatografía Líquida de Alto Rendimiento
y Detección UV.